2025.12.02 トピックス
宇宙における創薬エコシステム|膜タンパク質解析が変える次世代医薬開発

Ⅰ.前提と要旨
地上の構造生物学では、現代創薬の主要なターゲットである「膜タンパク質」の解析が依然として難題となっている。私たちが住む地球という重力環境下では対流や沈降により結晶の秩序が乱れ、構造解析に必要な高品質結晶を得にくい。その結果、簡単に言えば、分子が小さい状態でしか得られず、分子標的薬のターゲットであるリガンドの正確な形状等が判明せず、これが分子標的薬の耐性機構の未解明や、AI創薬の学習データ不足につながっている。
微小重力環境を利用したタンパク質の結晶化への取り組みは、この課題を突破する現実的な手段として注目される一方、ロジスティクスをはじめ・IP・契約・安全管理・宇宙法など、科学以外の課題が絡み合う複合領域でもある。私たちJapan Healthcare Solutionsがこれらを統合し、科学・制度・ビジネスを貫く“トランスレーター”としてのガバナンスを設計することで、宇宙を創薬インフラの一部として社会に根づかせることを支援していく。
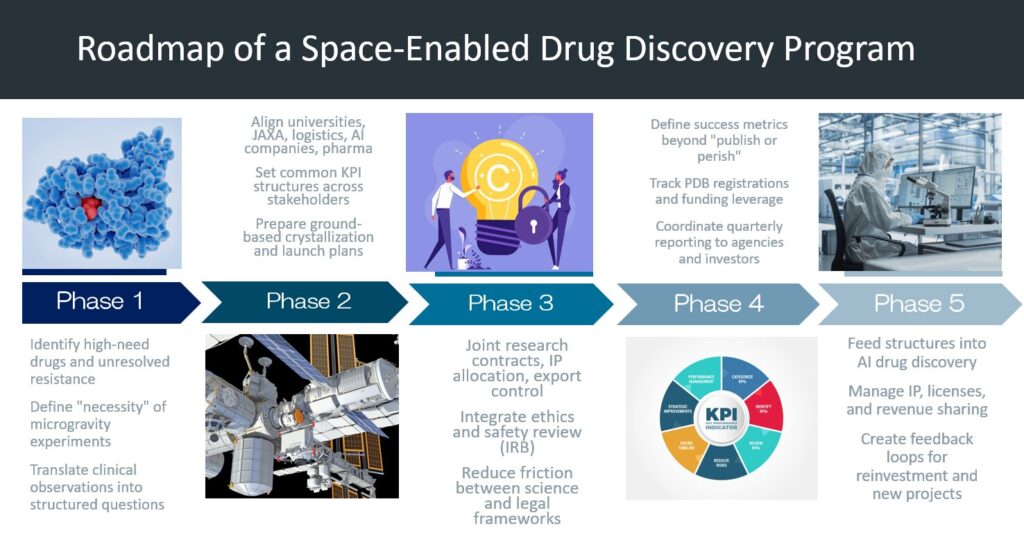
Ⅱ.社会実装に向けたフェーズ構成
フェーズ1:科学的仮説の社会化
臨床現場で耐性やMutation(変異)が報告される既存の分子標的薬等、または地上で結晶化が困難な「膜タンパク質群」を抽出・特定し、宇宙で解析する「必然性」を論理的に整理する。
説明がしやすい例で言えば、CML(慢性骨髄性白血病)治療薬である「イマチニブ」(ノバルティス社)が挙げられる。イマチニブは、当時、致死率が低くはなかったCMLに対する特効薬として開発された医薬品史を代表する分子標的薬であり、当時はノバルティス全体を支える屋台骨の一つとして、1錠の薬で年間数兆円を稼ぎあげるブロックバスターであった。イマチニブは白血病治療の歴史に大転換を与え、95%以上の患者のOS(生命予後)が10年をゆうに超え、分子遺伝学的完全寛解 (CMR)を達成する症例が続出、その構造式の根源の解明はラスカー賞やガードナー国際賞など、数々の賞を受賞した。
しかし、どうしても治療中に重大なSide Effectが発生し脱落しなければならない症例や、耐性が生じる患者群が存在した。臨床現場では国際チームが組まれ「どのような背景を持った患者群にイマチニブは効果を発現し、どのような背景の患者には耐性が生まれるのか?」を特定する研究が活発に行われた。これは、イマチニブの後の後継新薬となる「ニロチニブ」においても、日本を含めた多国共同研究が行われた。ニロチニブも優れた医薬品で、国際標準化スケールでモレキュラーレスポンス4.5以上、つまり血中のがん細胞が0.0032%未満になる割合はイマチニブを圧倒し、事実上の完治に近い寛解が長期に得られた。それでも耐性が出て急性増悪後、死に至る症例群は一定数存在し、臨床現場では国際チームが数年をかけて共同研究をしても、一向に原因が特定できなかった。
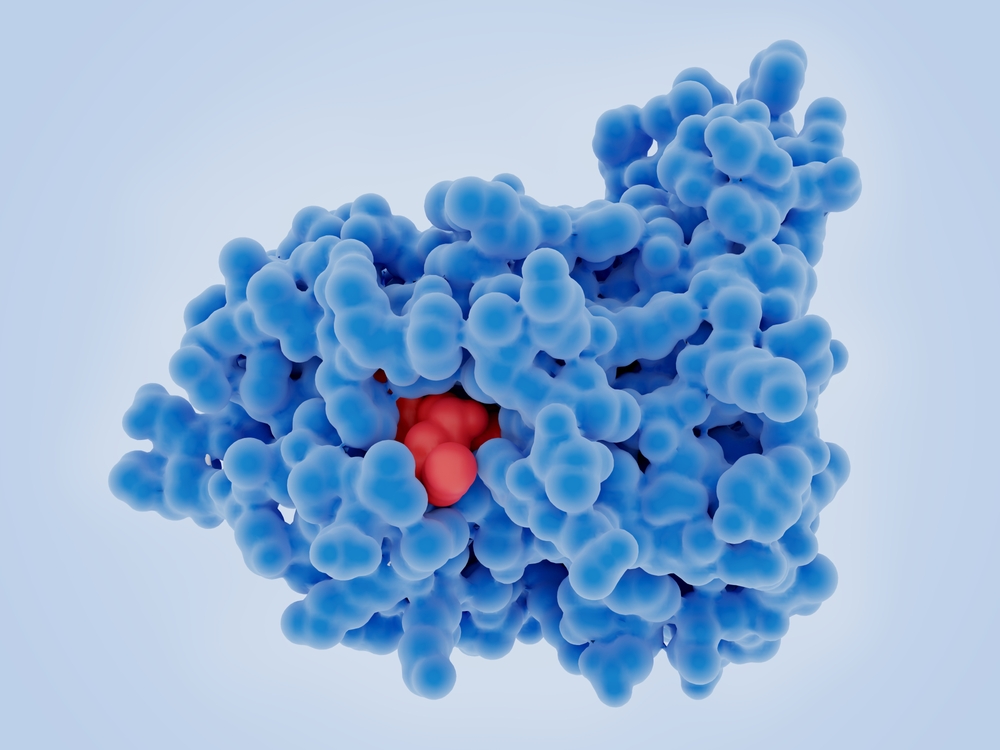
もし仮に、ここで原因の特定ができていれば、昨今医療費の逼迫で叫ばれている「個別化医療」の先駆けとなる優れた研究成果となったはずだった。
しかし、20年近い時を経て、JAXAやNASAなどの技術革新や、ISS国際宇宙ステーションでの実験ラボの充実、民間への門戸の開放政策等から、宇宙へのアクセスが飛躍的に容易になった。そこで可能となったのが、イマチニブ・ニロチニブのような医薬品のseedsである膜タンパク質を宇宙に飛ばし、大きく育ったタンパクの構造が解明の容易性を高めた結果、耐性の原因が、実は膜タンパク質表面のリガンド(タンパクと医薬品が結合する鍵穴のようなもの)の形状と、医薬品の鍵側の形状が僅かに異なることにあった事実が解明できるようになった。
つまり、何年かけても世界中で解明することができなかった分子標的薬の耐性患者背景の、その「答えが宇宙にある」のだ。医薬品開発チームは、この新たなタンパクのリガンド情報に基づき、新たな構造式を持つ医薬品を開発することで、耐性の出ない画期的な新薬の誕生に直結させることができるようになる。
弊社Japan Healthcare Solutionsは、ヘルスケア・ライフサイエンスに専門特化するコンサルティングファームであり、科学的な判断を下す立場ではない。しかし、膨大な医学論文などの臨床データやPDB空白領域をもとに、
①需要が極めて高い医薬品で、
②一定の耐性が生じており、
③耐性原因探求のための地上で研究に限界があり、
④宇宙に飛ばすことでその原因が解明しやすい医薬品候補で、
⑤開発可能性が高く、
⑥薬事承認やその後の上市販売含めてスケール化が可能な、
いわゆる「勝ち筋」を絞り込むことができる。要は、研究機関と共同で“社会実装の前提としての研究仮説”を形成するのだ。
〈我々の役割〉
候補となるリストを整理し、研究者との議論の“トランスレーター”を務める。科学的根拠を社会・経済・制度の文脈に置き換え、研究テーマを「政策的・経済的に成立する問い」へ変換する。
〈フェーズKPI例〉
・候補タンパク質リスト:3〜5件確定/・「宇宙利用の必然性」文書化率:100%/・研究仮説形成に関与した研究機関数:2件以上
フェーズ2:エコシステム設計と具体化(タンパク変異体の例)
宇宙実験には、JAXA・大学・民間バイオ企業・AI企業・ロジスティクス・法務・保険など多数の主体が関与する。したがって、宇宙での創薬は、製薬メーカー単独では大変困難である。我々はそれらの目標とリスクを整理し、“共通KPI構造”に落とし込む。
【実施イメージ】
たとえば、非小細胞肺がんのEGFR耐性変異(C797S)を対象とする場合、我々は臨床データと論文情報を整理し、大学・研究機関に地上での予備結晶化試験体制を整備する。同時に、JAXAや宇宙輸送企業と打ち上げ・回収スケジュールを調整する。この段階で重要なのは、科学的内容ではなく、科学を動かす制度の整備である。共同研究契約、発明者帰属、輸出管理、安全審査、倫理審査の手順を我々がまとめ、研究者が実験に集中できる環境を作る。
打ち上げ後、回収された結晶は理研・大学が解析を担い、得られた構造はAI創薬モデルに組み込まれる。製薬企業はそのデータを使ってリガンド再設計を行う。そして非常に大きな副次的効果の一つが、行政が公的研究費の社会的リターンを可視化できること、そして上市後の生命予後や治療費等から社会保障費抑制の逆算が可能になることである。我々はその全工程で、関係者間の合意形成とKPI連動の制度設計を統括する。
〈我々の役割〉
科学者と行政・企業の間で“トランスレーター”を務め、異なるKPI(論文/利益/公共性)を整合させる。契約交渉、費用分担、成果配分を制度化する。
〈フェーズKPI〉
・MOU・契約締結数:3機関以上/・各主体のKPI明文化率:100%/・法的審査・輸出管理承認:100%

フェーズ3:制度化と法的整備
科学を社会に接続する段階で、最も多くの誤解が生じるのが「リーガルvsサイエンスの境界」である。我々は法的助言を直接行うのではなく、外部法律顧問・知財専門家・倫理委員会との調整窓口として機能する。つまり、「契約を作る側」ではなく、「専門家と研究現場を正しくつなぐ側」として動く。
この分業により、科学者が複雑な法制度に巻き込まれずに研究を進められ、法律家も科学の文脈を誤解せずに助言できる。共同研究・知財契約は外部弁護士と連携し、雛形と実務ルールを整備する。倫理・安全審査は各機関のIRBを束ね、重複審査を防止する。宇宙法・輸出管理はJAXA・法務局・外部顧問と三者調整で進めることとなる。
〈我々の役割〉
各領域の専門家の「翻訳と橋渡し」。科学・法律・行政の三言語を理解し、誤解なく情報を流す“交通整理役”。
〈フェーズKPI〉
・契約雛形整備率:100%/・専門家連携協定締結数:3件以上/・トラブル・遅延件数:0件
フェーズ4:KPI設計と成果評価
KPIは、ゴールから逆算して設計することが重要である。最終目標(ex, 膜タンパク質構造5件登録)を前提に、「その成果を生む環境」の整備度を測る。候補確定件数3〜5件、参画契約数3件以上、共通データ共有プロトコル整備率100%、外部資金誘発倍率1.5倍などを設定し、「科学の成否」ではなく、「科学が進む条件の保証を制度指標として管理」する。これまで、時としてこのKPIを巡って対立し合う関係にあった。つまり、ビジネスでは早期にマネタイズできる研究群に投資をするのは当然であり、一方で、科学ではその投資に見合う成果が生まれる可能性を担保又は高めることは困難であった。これを「勝ち筋」Seeds群の分析と特定、薬事や法務、市場規模等とのトランスレーターを我々が行うことで、投資家が納得するより合理的・効率的な「勝ち筋の見える科学」として実装することができるようになる。
〈我々の役割〉
KPIの策定とトラッキング、報告書作成。AMED・JAXA・投資機関への報告書を統一形式で取りまとめる。
〈フェーズKPI〉
・KPI設計・承認完了:100%/・四半期報告の提出率:100%/・投資家・行政の満足度評価:90%以上
フェーズ5:社会実装と再投資
宇宙で得られたデータはAI創薬にフィードバック又は応用され、製薬・政策・投資のサイクルの中に組み込まれる。我々は成果報告・知財管理・収益配分を透明化し、次フェーズへの再投資を、根拠を持って誘導する。外部法律顧問・知財事務所・金融機関と連携し、知の還元と利益の分配を両立させる。
〈我々の役割〉
データ帰属・特許・ライセンス契約の橋渡し、政策提言・再投資ファンド設計、社会実装報告の取りまとめ。
〈フェーズKPI〉
・PDB登録:5件(ゴール)/・特許・ライセンス収益化:2件以上/・再投資誘発倍率:1.5倍/・関連プロジェクト立ち上げ:2件以上
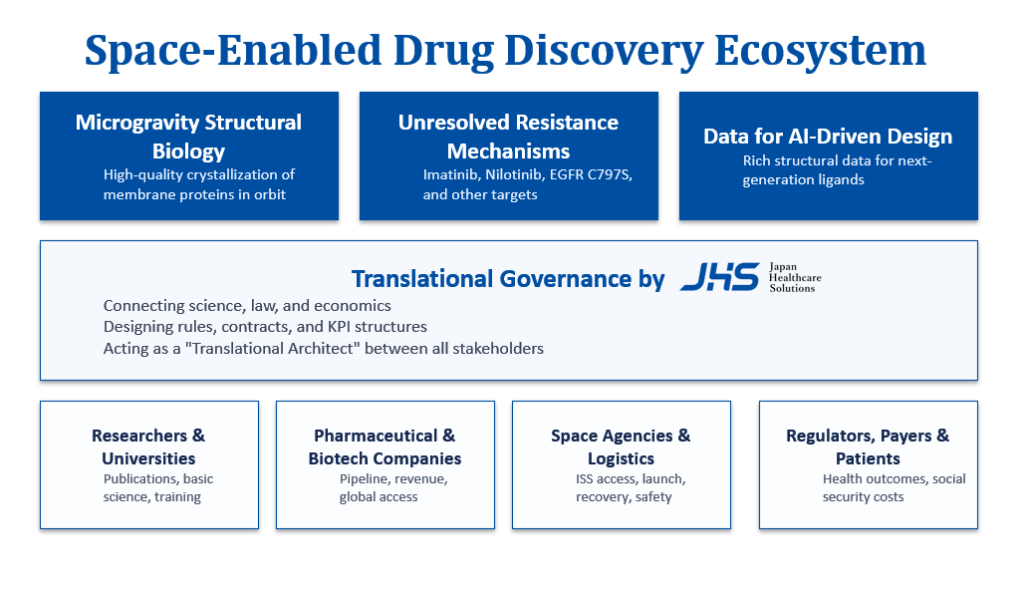
Ⅲ.エコシステムの必要性と相互便益
宇宙実験は単独では成立しない。研究者、企業、行政、法律家、輸送業者、それぞれのKPIと責任が異なる。その差異を調律し、互いの専門性を損なわずに連携できる制度構造を作るのが我々の役割である。近年、どのコンサルティングファームでも、少子高齢化による国内市場規模の縮小に課題意識は高まっている。しかし、実際には「クロスインダストリー」を描くことに各社難渋している。医療は、製薬メーカーだけでなく、医療現場・介護・政策・患者が複合的に絡み合う世界であり、これらが全て同じ速度で動くことで初めて、社会実装ができる。しかし、従来のコンサルファームは、案件金額が大きな製薬案件こそ得意で、組織体制効率化や治験DX等こそ進んだものの、それ以外の「生活者」や「社会インフラ」が置いて行かれてしまっているのだ。それは、従来コンサルファームが、案件金額が大きな製薬メーカーに依存していた経緯が深く関係する。その結果、社会実装を試みるクライアントに対しても、単なる”PoC死“のようなコンサルティングレポートを提供するしかなく、クライアントもこれを信じるしかない悪循環が発生している。これを脱却するためには、HLSを起点にしつつ多様な産業に精通したクロスインダストリーファームの存在が必要であることは、明らかである。
Ⅳ.権利と法的留意点
宇宙におけるエコシステム及び共同開発となると、宇宙に飛ばすことそのものの価値が非常に高くなる。つまり、製薬メーカーや大学単体では困難なことを、宇宙のロジスティクスカンパニーがいるからこそ実行できる。このように、強い力をもつステークホルダーが絡み合う瞬間、その権利(知財権等について)揉めることは少なくない。しかし、互いの利害を整理し、短期・中期的な目標さえ一致させることができれば、この混乱は収めることができる。ZOPA・BATNAを明確に設定・設計せずして、エコシステムを組んでしまうことで、後々ハレーションが起きるのであって、この設計を明確なものとし、エコシステムのステークホルダー誰もが利益を得られるアライアンスにすることもまた、コンサルティングファームの「オーケストレーター」としての重要な役割なのである。
〈我々の役割〉
・共同発明契約と使用権の明確化
・ITAR/EARおよび宇宙条約への適合
・IRB・安全審査の一本化と責任範囲の明示
・データの二次利用・公開ルールの透明化
Ⅴ.我々の役割(総括)
我々は科学そのものを担わず、法律を独占的に扱うわけでもない。だが、その二つの世界を安全に、効率的に、相互に理解させるアーキテクターとして機能する。科学領域では研究者とのコミュニケーション支援と社会的意義の翻訳、制度領域では契約・倫理・法務の全体設計と外部顧問との連携、経済領域では資金循環・知財・再投資の設計と管理、そして全体調整としてKPIの可視化と合意形成を担う。
Ⅵ.結語
本プロジェクトの目的は、宇宙を「実験空間」から「社会設計の舞台」に変えることだ。科学を終点にせず、制度・法務・経済の言語で社会に接続する。我々はそのトランスレーターまたはアーキテクターの役割を担い、科学者・行政・企業・法律家をつなぐ“架け橋役”として、宇宙利用創薬の社会実装を現実にしていく。
最後に、コンサルティングファーム業界への提言をさせていただく。コンサルティングファームでは、組織が大きいほど、所謂「即時儲かる旧来の安定型プロジェクト」しか受託ができず、一方で、現状のままでは、これまでのアドバイザリーとしての付加価値が減耗低迷する。しかし、今日明日の売上を稼ぎ上げることのみに集中してしまっては、結果として、例えば大手製薬メーカーのMR営業部門の構造変更プロジェクトを提案してみたり、業務DX化案件などを同じスキームで繰り返すだけになり、そこにコンサルティングファームとしての付加価値やノウハウの蓄積が生まれない。もちろん、伝統的なネットワークを持つ医療産業へ的確なアドバイスを伝え成功に導くことは重要なミッションであり、且つ自社自身も稼ぎ上げることは必要だ。しかしながら、イノベーションを語るコンサルティングファーム自身が、イノベーションを起こしづらい環境に陥っていること(イノベーションのジレンマ)も、事実として見えている。
コンサルティングファームのミッションとは、今を稼ぎ上げ自社のサステナビリティを確保すると共に、本例のように、未来への投資・イノベーションに懸けた投資的活動もまた一つなのではないだろうか。言い換えれば、エコシステムを構築し、理論や証拠や法的役割に基づき、各機関の強みや弱みを相互に折り重ね、共同体として一つのイノベーションを引き起こすアーキテクターとなることだと筆者は考える。

